Молекулярна і структурна формула метану
Молекулярна, структурна і електронна формуламетану складаються на основі теорії будови органічних речовин Бутлерова. Перш ніж приступати до написання таких формул, почнемо з короткої характеристики даного вуглеводню.

особливості метану
Дана речовина є вибухонебезпечним, його щеіменують «болотним» газом. Специфічний запах цього граничного вуглеводню відомий всім. У процесі згоряння від нього не залишається хімічних компонентів, які впливають на організм людини. Саме метан є активним учасником освіти парникового ефекту.
Фізичні властивості
Перший представник гомологічного ряду алканівбув виявлений вченими в атмосфері Титана і Марса. З огляду на той факт, що метан пов'язаний з існуванням живих організмів, з'явилася гіпотеза про існування життя на цих планетах. На Сатурні, Юпітері, Нептуні, Урані, метан з'явився в якості продукту хімічної переробки речовин неорганічного походження. На поверхні нашої планети його зміст незначне.

Загальна характеристика
Метан не має кольору, він легший за повітря майже вдва рази, погано розчиняється у воді. У складі природного газу його кількість досягає 98 відсотків. У нафтовому попутному газі міститься від 30 до 90 відсотків метану. Більшою мірою метан має біологічне походження.
Копитні травоїдні кози та корови випускають припереробці в шлунках бактерій досить значну кількість метану. Серед важливих джерел гомологічного ряду алканів виділимо болота, термітів, фільтрацію природного газу, процес фотосинтезу рослин. При виявленні на планеті слідів метану, можна говорити про існування на ній біологічного життя.

способи отримання
Розгорнута структурна формула метану єпідтвердженням того, що в його молекулі тільки насичені одинарні зв'язки, утворені гібридними хмарами. Серед лабораторних варіантів отримання даного вуглеводню відзначимо сплав ацетату натрію з твердим лугом, а також взаємодія карбіду алюмінію з водою.
Горить метан блакитним полум'ям, виділяючи прице близько 39 МДж на кубічний метр. Вибухонебезпечні суміші дана речовина утворює з повітрям. Найбільш небезпечний метан, який виділяється під час проведення підземних розробок родовищ корисних копалин в гірських шахтах. Високий ризик вибуху метану і на збагачувальних вугільних і брикетних фабриках, а також на сортувальних виробництвах.
Фізіологічна дія
Якщо процентний вміст метану в повітрістановить від 5 до 16 відсотків, при попаданні кисню можливе займання метану. У разі істотного зростання в суміші цієї хімічної речовини підвищується ймовірність вибуху.
Якщо в повітрі концентрація даного алкана становить 43 відсотки, він є причиною задухи.
Під час вибуху швидкість поширення становить від 500 до 700 метрів в секунду. Після того як метан контактує з джерелом тепла, процес займання алкана відбувається з деяким запізненням.
Саме на цій властивості базується виробництво вибухобезпечного електричного обладнання та запобіжних вибухових компонентів.
Так як саме метан є термічностійким насиченим вуглеводнем, він має широке застосування в вигляді промислового і побутового палива, а також використовується в якості цінної сировини для хімічного синтезу. Структурна формула три-етил-метану характеризує особливості будови представників даного класу вуглеводнів.
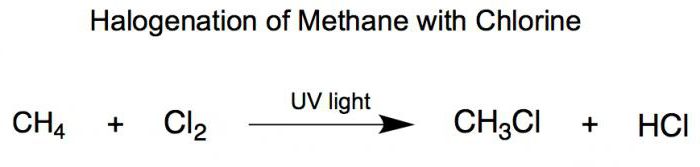
У процесі його хімічної взаємодії зхлором при впливі ультрафіолетового опромінення можливе утворення декількох продуктів реакції. Залежно від кількості вихідної речовини, можна в ході заміщення отримати хлорметан, хлороформ, чотирихлористий вуглець.
У разі неповного згоряння метану утворюється сажа. У разі каталітичного окислення утворюється формальдегід. Кінцевим продуктом взаємодії з сіркою є сірковуглець.
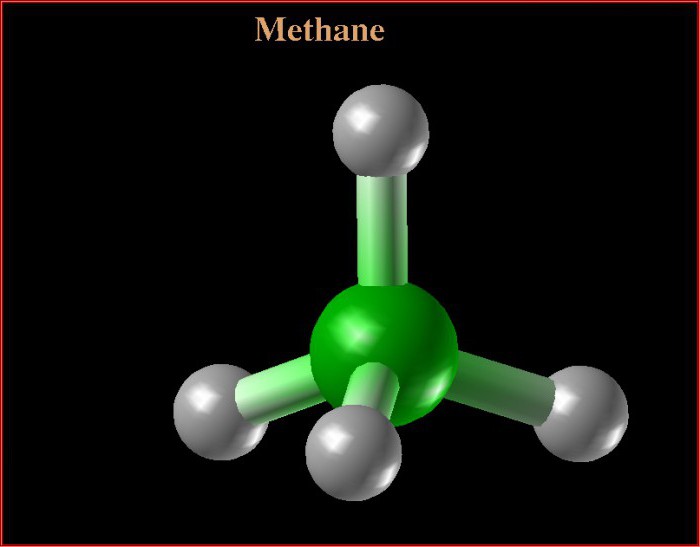
Особливості структури метану
Яка його структурна формула? Метан відноситься до граничних вуглеводнів, які мають загальну формулу СnН2n + 2. Розглянемо особливості утворення молекули, щоб пояснити, як утворюється структурна формула.
Метан складається з одного атома вуглецю і чотирьох атомів водню, пов'язаних між собою ковалентним полярної хімічним зв'язком. Пояснимо на основі будови атома вуглецю структурні формули.
вид гібридизації
Просторова будова метану характеризуєтьсятетраедричних структурою. Так як на зовнішньому рівні у вуглецю чотири валентних електрони, при нагріванні атома відбувається перехід електрона з другої s-орбіталі на p. У підсумку на останньому енергетичному рівні у вуглецю розташовується чотири неспарених ( «вільних») електрона. Повна структурна формула метану грунтується на тому, що відбувається утворення чотирьох гібридних хмар, які орієнтуються в просторі під кутом 109 градусів 28 хвилин, формуючи структуру тетраедра. Далі відбувається перекривання вершин гібридних хмар з негібридних хмарами атомів водню.
Повна і скорочена структурна формула метану вповною мірою відповідає теорії Бутлерова. Між вуглецю і водню утворюється проста (одинарна) зв'язок, тому для цієї хімічної речовини не характерні реакції приєднання.
Нижче представлена кінцева структурна формула. Метан - це перший представник класу насичених вуглеводнів, він володіє типовими властивостями граничного алкана. Структурна та електронна формула метану підтверджують тип гібридизації атома вуглецю в даному органічній речовині.

Зі шкільного курсу хімії
Даний клас вуглеводнів, представникомякого є «болотний газ», вивчається в курсі 10 класу середньої школи. Наприклад, хлопцям пропонується завдання наступного характеру: «Напишіть структурні формули метану». Необхідно розуміти, що для цієї речовини можна розписати по теорії Бутлерова тільки розгорнуту структурну конфігурацію.
Його скорочена формула буде збігатися змолекулярної, записуватися у вигляді СН4. За новим федеральним освітнім стандартам, які введені в зв'язку з реорганізацією російської освіти, в базовому курсі хімії всі питання, що стосуються характеристики класів органічних речовин, розбираються оглядово.
промисловий синтез
На основі метану були розроблені промисловіспособи такого важливого хімічного компонента, як ацетилен. Основою термічного і електричного крекінгу стала саме його структурна формула. Метан при каталітичному окисленні з аміаком утворює синильну кислоту.
Застосовують даний органічна речовина длявиробництва синтез-газу. При взаємодії з водяною парою виходить суміш чадного газу і водню, що є сировиною для виробництва граничних одноатомних спиртів, карбонільних сполук.
Особливе значення має взаємодія з азотною кислотою, в результаті виходить нитрометан.

Застосування у вигляді автомобільного палива
У зв'язку з нестачею природних джерелвуглеводнів, а також збіднінням сировинної бази, особливої актуальності набуває питання, пов'язане з пошуком нових (альтернативних) джерел для отримання палива. Одним з таких варіантів є біодизельне паливо, в складі якого є і метан.
З огляду на різницю в щільності між бензиновимпаливом і першим представником класу алканів, існують певні особливості застосування його в якості джерела енергії для автомобільних двигунів. Для того щоб не було необхідності перевозити з собою величезну кількість метану, шляхом стиснення його щільність збільшують (при тиску близько 250 атмосфер). Зберігають метан в зрідженому стані в балонах, що встановлюються в автомобілях.
Вплив на атмосферу
Вище вже йшла мова про те, що метан надаєвплив на парниковий ефект. Якщо ступінь дії оксиду вуглецю (4) на клімат береться умовно за одиницю, то в ньому частка «болотного газу» становить 23 одиниці. Протягом двох останніх століть вчені спостерігають підвищення кількісного вмісту метану в земній атмосфері.
На даний момент приблизну кількість СН4 оцінюється в 1,8 частини на мільйон. Незважаючи на те що даний показник в 200 разів менше, ніж наявність вуглекислого газу, йде розмова між вченими про можливий ризик утримання тепла, випромінюваного планетою.
У зв'язку з відмінною теплотворною здатністю «болотного газу», його застосовують не тільки в якості вихідної сировини при здійсненні хімічного синтезу, але і як джерело енергії.
Наприклад, на метані функціонують різноманітні газові котли, колонки, призначені для індивідуальної опалювальної системи в приватних будинках і заміських котеджах.
Такий автономний варіант опалення вельми вигіднийдля власників житла, не пов'язаний з аваріями, систематично відбуваються на централізованих опалювальних системах. Завдяки газового котла, що функціонує на даному виді палива, достатньо 15-20 хвилин для того, щоб повністю обігріти двоповерховий котедж.
висновок
Метан, структурні та молекулярні формулиякого були наведені вище, є природним джерелом енергії. Завдяки тому, що в його складі є тільки атом вуглецю і атоми водню, екологи визнають екологічну безпеку даного насиченого вуглеводню.
При стандартних умовах (температурі повітря 20 градусів за Цельсієм, тиску 101325 Па) ця речовина є газоподібним, нетоксичним, нерозчинним у воді.
У разі зниження температури повітря до -161 градуси, відбувається стиснення метану, що широко застосовують в промисловості.
Метан впливає на здоров'я людини. Він не є отруйною речовиною, але вважається задушливим газом. Існують навіть граничні норми (ГДК) за змістом цієї хімічної речовини в атмосфері.
Наприклад, роботи в шахтах дозволені тільки в тихвипадках, коли його кількість не перевищує на метр кубічний 300 міліграмів. Аналізуючи особливості будови даного органічної речовини, можна зробити висновок про його схожості з хімічним і фізичним властивостям з усіма іншими представниками класу насичених (граничних) вуглеводнів.
Ми проаналізували структурні формули, просторова будова метану. Відповідний ряд, який починає "болотний газ", має загальну молекулярну формулу СnН2n + 2.